腹部・腫瘍系IVR
「はじめに」
Interventional Oncologyはがん治療において外科手術、化学療法、放射線治療に続く4本目の柱として大きな役割を担っており、治療デバイスや治療支援ソフトウエアといった機器の発達と共に患者さんや他科からの期待はますます高まっています。そうした中、私たち奈良医大Oncologyチームは院内各専門領域の医師からの直接依頼はもちろんのこと、全国の病院からがん症例に関してコンサルテーションを受け、信頼を得ています。
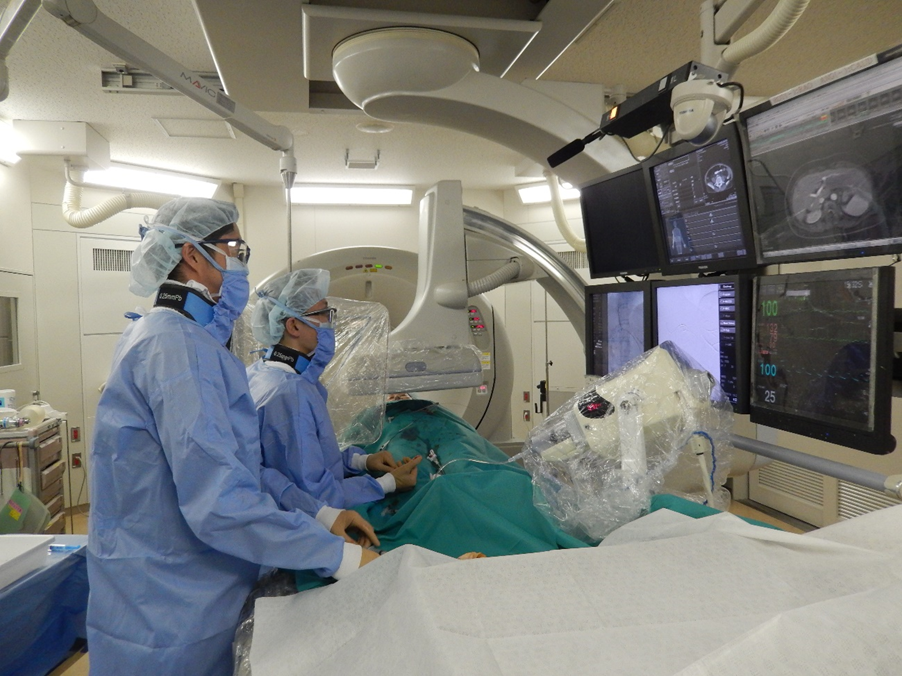
これらを可能にしているのが、IVRセンターと放射線科病棟です。当センターの1階には5台のIVR専用の血管造影装置(心血管用2台を含む)とIVR-CT 1台が設置され、2階にはIVRと外科手術を同時に施行可能であるハイブリッド手術室が導入されています。加えて、当科では放射線科病棟を有し、外来から入院まで責任をもってがん患者さんのサポートを行っています。実際にはOncology領域の血管系、非血管系IVRのみならず子宮筋腫や内蔵動脈瘤、血管奇形などの塞栓術、外来CVポート留置や外来生検など広範囲のIVRを手掛けていますので、Oncology領域以外の疾患でもご紹介頂くことが可能です。
「臨床」
肝細胞癌に対するTACE
肝動脈化学塞栓療法 (Transarterial chemoembolization; TACE)には本邦で開発されたリピオドールを用いたTACE(cTACE)と欧米で開発されたマイクロスフィアを用いたTACE(DEB-TACE)があります。奈良医大放射線・核医学科では、本邦におけるTACEの先駆者として、基礎研究から臨床研究に至るまで様々な研究を実施しています。
転移性肝腫瘍
1)ラジオ波焼灼療法(RFA)/マイクロ波焼灼療法(MWA)
焼灼療法は、開腹手術で腫瘍を摘出するのと同等の効果があるとすでに世界中で報告されています。奈良医大放射線・核医学科においても積極的に根治を目指した治療を取り入れています(図1)。
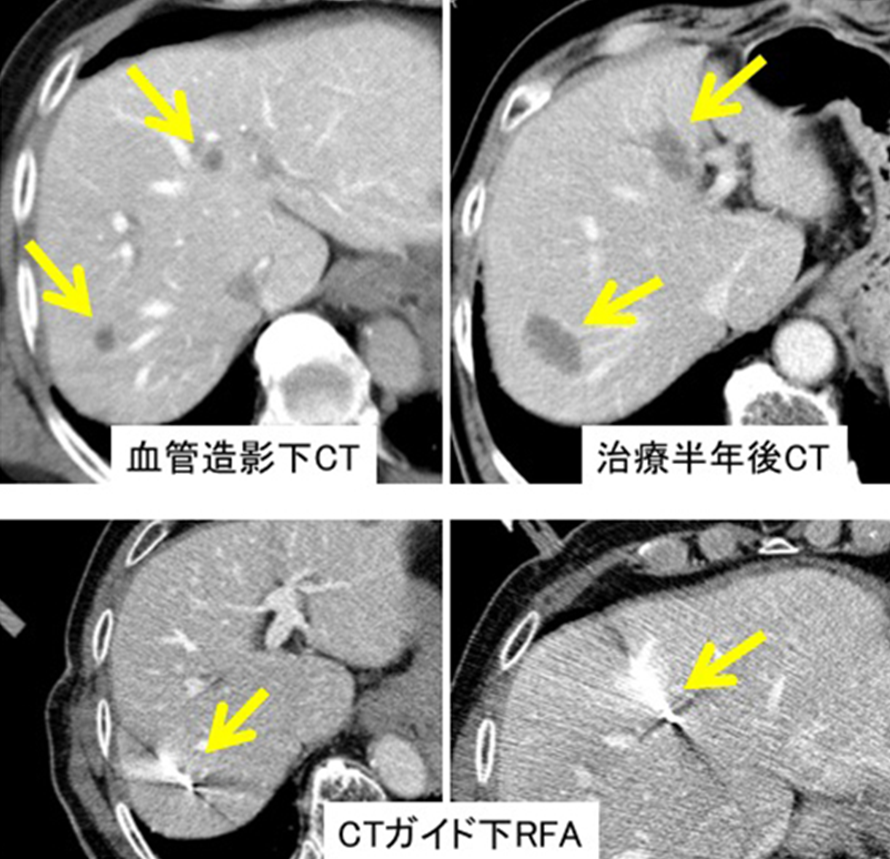
図1:超音波では同定できないような小さな転移結節であっても血管造影下CTを用いることで病変を正確に同定し、安全に高い精度で治療を完遂した症例
2)肝動注リザーバー療法
肝動注リザーバー療法は、肝臓へ直接抗がん剤を注入することで良好な腫瘍の縮小効果が得られます。当院では、以下の症例に対して、積極的に実施しています (図2)。
1.肝機能に影響がでるほど高度に進行した症例
2.縮小させ外科的切除に移行したい症例
3.高齢などの理由で通常の全身化学療法に耐えられない症例
4.副作用が強いため全身化学療法が継続できない症例
5.すでに全身化学療法を受けられ(現在受けておられ)、十分な効果が得られていない症例
治療は原則として外来通院で行いますが、病態や生活状況によって適宜入院での対応をしています。
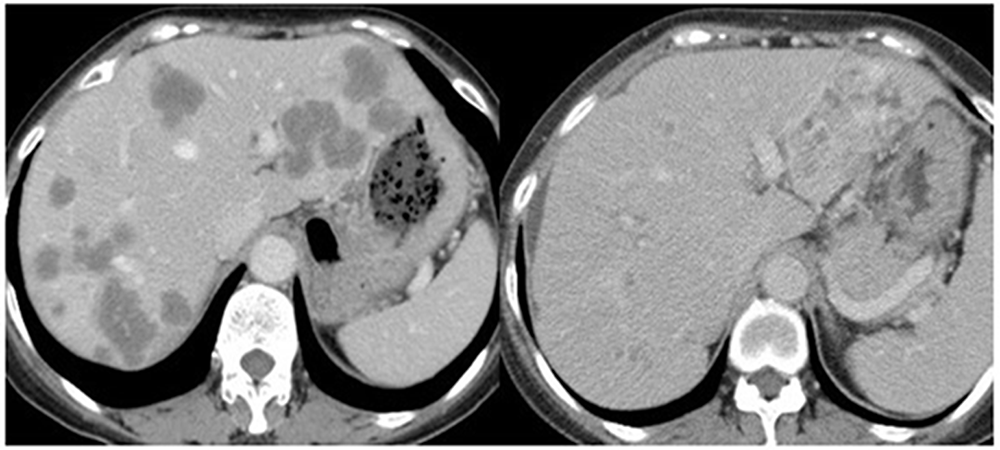
図2:肝内に多発する転移病変に対して動注療法を継続し、腫瘍の著明な縮小が得られた症例
3)肝動脈化学塞栓療法
近年、奈良医大放射線・核医学科では微小デンプン球と抗がん剤を混和した新たな動注療法を開発し、優れた治療効果が得られることを臨床試験で確認しました。
我々の臨床データでは、全身化学療法で抗がん剤が効かなくなった方を対象として、61%で腫瘍の著明な縮小を得ることができました。
また、欧米で開発された球状塞栓物質(ビーズ)を用いた動脈塞栓療法を転移性肝腫瘍の症例に行っています。
ビーズは100〜300μmのものを用いますが、腫瘍の状態によってビーズのサイズの使い分けをしています。
IVRのカテーテル技術を用いて腫瘍にだけビーズを注入することで副作用を抑えることが可能であり、様々な症例に対応しています。
膵癌に対する経カテーテル治療
奈良医大放射線・核医学科では約15年前より膵癌に対する経動脈的カテーテル治療の臨床・研究に取り組んできました。臨床では、動注リザーバーを用いた膵原発病巣および肝転移に対する動注化学療法や薬剤溶出性ビーズや可溶性微少デンプン球を用いた肝転移のTACEを行っています。
「教育」
当院では充実した教育体制を築いています。日常診療で遭遇したIVR症例によるcase based discussionのほか、臨床テーマによる論文作成の指導など行っています。また、全国のIVR技術向上を目的に1年間を通して定期的にワークショップを開催しており、これまで国内の意欲あるIVR医に多数ご参加頂いています。紙面のみでは伝えきれない部分もありますので、ぜひ見学に来て当科の良さを味わって下さい。
「学術」
研究面では、近年特に動物実験を主体としたOncologyに関する基礎研究を精力的に行っており、国内外から高い評価を得ています。
肝細胞癌
1)画像支援技術を用いた高精度なTACE
画像診断技術が発達・普及している本邦では、早期の肝細胞がんを見つけることが可能である一方、腫瘍の栄養血管の決定は、血管造影技術のみでは腫瘍の大きさ、腫瘍が存在する区域、あるいはその血流程度によって困難なことがあります。当院では、選択的DSAやCTHA画像を用いて、3D構成した融合画像(fusion-MIP imaging)を作成し、栄養血管の同定を行い精度の高い手技を提供しています(図1)。また、これらのプロトコールを独自に開発したことで、TACEをより高精度にかつ迅速に実施することが可能となっています。現在、技術の普及に向けてソフトウエアの開発を臨床研究として進めています。
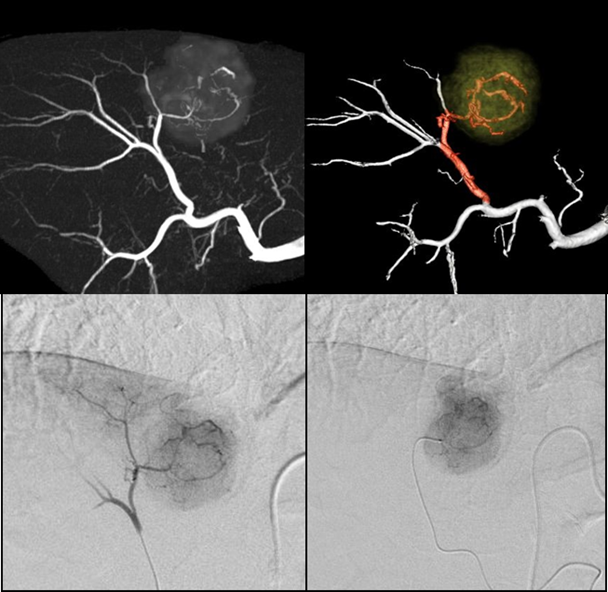
図1.fusion-MIPとDSAで栄養血管を推定し、TACEを施行
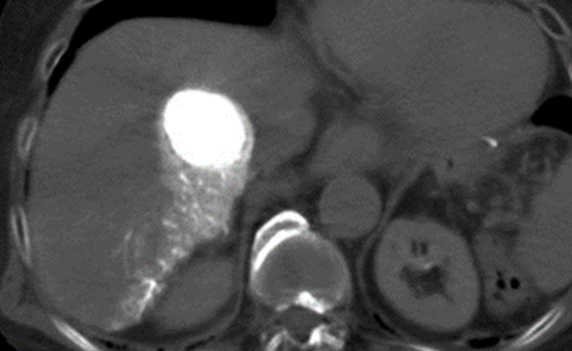
TACE後CT画像 腫瘍に良好なリピオドール沈着を認める。
2)3D-safety marginを獲得し局所効果を高めるTACE
局所制御や予後において、腫瘍のマージンを獲得することは、切除術やRFAにおいて最も重要な技術的因子の一つと考えられています。TACEにおいても様々な技術的因子が報告されてきた中で、腫瘍を包括するようなマージン(3D-safety margin)を獲得することは、局所制御だけでなく予後因子としても重要であることを我々は、報告してきました(図2;現在論文投稿中)。様々な原因で切除術やRFAが施行できない症例においても、超選択的cTACEにより根治を目指し、切除術やRFAに匹敵する成績を目指しています。 局所制御や予後において、腫瘍のマージンを獲得することは、切除術やRFAにおいて最も重要な技術的因子の一つと考えられています。TACEにおいても様々な技術的因子が報告されてきた中で、腫瘍を包括するようなマージン(3D-safety margin)を獲得することは、局所制御だけでなく予後因子としても重要であることを我々は、報告してきました(図2;現在論文投稿中)。様々な原因で切除術やRFAが施行できない症例においても、超選択的cTACEにより根治を目指し、切除術やRFAに匹敵する成績を目指しています。
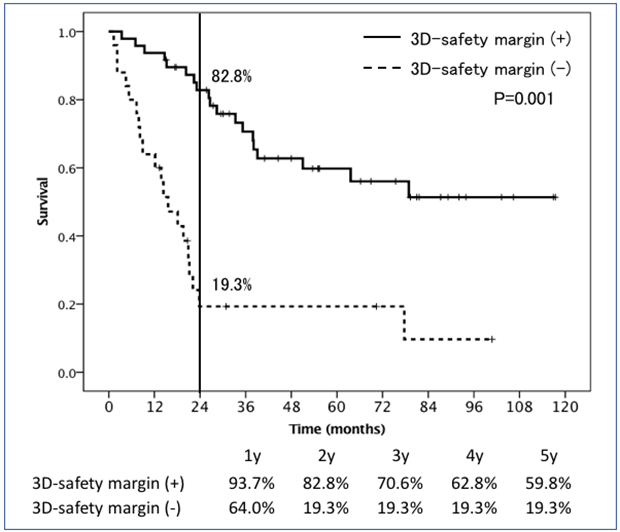
図2. 3cm以下単発肝細胞癌に対する局所無再発率のグラフ
3)高齢者や肝機能不良例に対する有効で安全なTACE
奈良医大放射線・核医学科では、80歳以上の超高齢者や肝機能が不良な方にも安全で有効なTACEを提供しています。このような症例におけるrisk factorについても臨床研究としてデータ解析を行い、DEB-TACEが適していることを報告してきました(現在論文投稿中)。今後は、cTACEとDEB-TACEにおいて両者の適正な位置付けを明確にし、発信していく予定です。
4)基礎研究と新たな治療法・機器の開発
ラットの肝細胞癌モデルを作成して、cTACEとDEB-TACEの効果の違いを組織学的、免疫学的に検討しています。また、放射線科医として、新たな画像診断法の開発や分子イメージング技術の応用を研究しています。ウサギの肝腫瘍モデルを作成し、新規抗がん剤の開発や既存の抗がん剤の有効性評価なども研究しています。
これらの結果を英語論文として多数報告し、海外学会で表彰され、また米国のがんセンターと共同研究を実施しています。
切除不能膵癌に対する動注療法
IVR-CTシステムを用いて進行膵癌の支配動脈が腹腔動脈と上腸間膜動脈の2重支配であることを明らかにし、これらの血管から5-FUを持続動注した臨床試験で良好な抗腫瘍効果(奏効率70%)が得られたことを報告しました。次に上腸間膜動脈から腫瘍へ流入する血流を遮断して腹腔動脈へ支配血管を一本化する血流改変術の基礎的・臨床的研究を行いました。その結果、膵癌の局所進展範囲から適応症例を選択すれば支配血管の一本化が実行可能であることが明らかなり、ブタを用いた基礎実験でこの方法の薬理学的有利性を証明しました。この手法を用いて行った第1/2相臨床試験では治療歴のない進行膵癌症例に対して奏効率約70%と高い腫瘍縮小効果が得られることを報告しました。現在、マイクロカテーテル挿入可能な埋め込み方ポートを開発し膵臓がんに対する臨床応用を目指す研究や、新規drug delivery systemを用いた膵臓がんに対する動物実験を行っています。
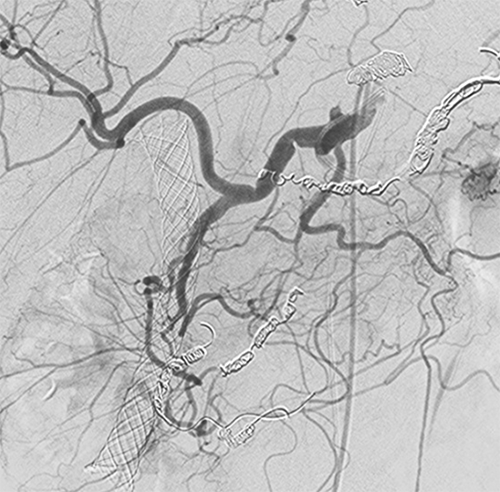
膵癌術後の予防的肝動注・膵癌肝転移に対するTACE
膵頭十二指腸術後における肝動注の安全性を評価した研究やコアキシャル法を用いたカテーテル留置術の臨床研究を行いました。
大腸癌肝転移
転移した病態に局所治療をする意義について、我々はこれまでに、化学療法抵抗性の症例に対して5-FUの肝動注療法を肝転移巣のみに行い、肝転移に効果がでた症例において生命予後が延長することを証明しました (下図)。
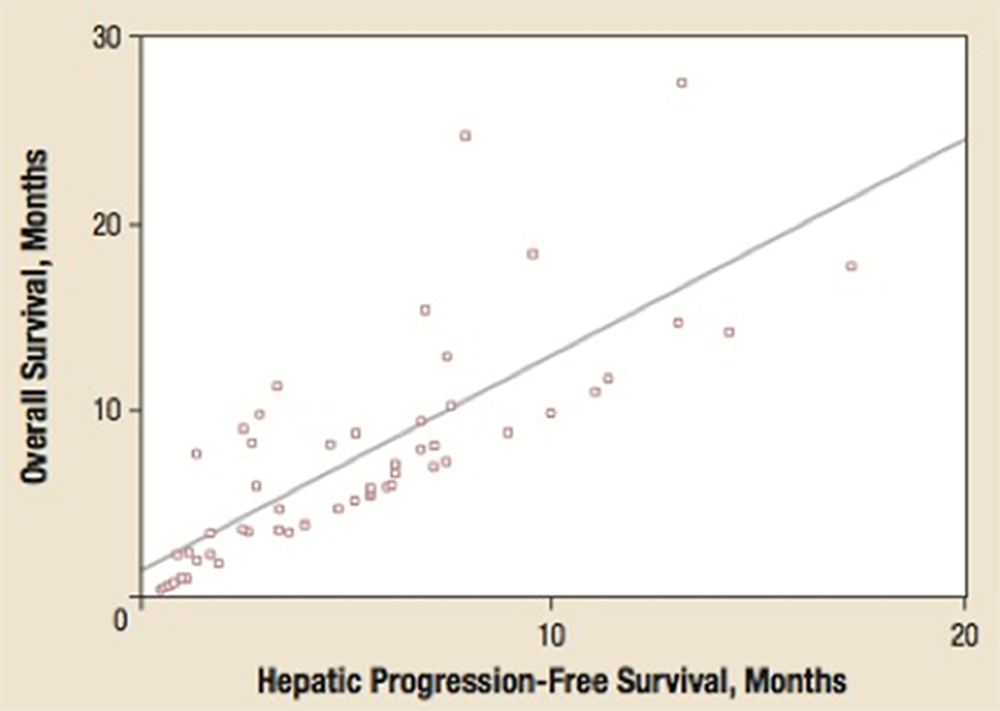
図:肝の制御が生存期間と強く相関する (Nishiofuku H, et al. Clinical colorectal cancer. 2010)
奈良医大での肝細胞癌に対するTACEの研究成果 (一部抜粋)
| 1. | Sato T, et al. Superabsorbent polymer microspheres prepared with hypertonic saline to reduce microsphere expansion. Cardiovasc Intervent Radiol 2018 (in press) |
| 2. | Tanaka T, et al. Development of pumping emulsification device with glass membrane to form ideal lipiodol emulsion in transarterial chemoembolization. Eur Radiol. 2018 May;28(5):2203-220. |
| 3. | Nishiofuku H, et al.Intraarterial Therapy Using Micellar Nanoparticles Incorporating SN-38 in a Rabbit Liver Tumor Model.J Vasc Interv Radiol 2017;28:457-464 |
| 4. | Fukuoka Y, et al. Compatibility of an Ultraselective Microcatheter and Epirubicin Loaded 300-500-μm DC Bead in Ex Vivo Study. Cardiovasc Intervent Radiol 2015;38:1284-7 |
| 5. | Tanaka T, et al. Superselective particle embolization enhances efficacy of radiofrequency ablation: effects of particle size and sequence of action. Cardiovasc Intervent Radio 2013;36: 773-782 |
奈良医大での膵がんに対する動注療法の研究成果 (一部抜粋)
| 1. | Hashimoto A. Tanaka T. Adjuvant Hepatic Arterial Infusion Chemotherapy for Pancreatic Cancer Using Coaxial Catheter-Port System. Cardiovasc Intervent Radiol. 2016;39:831-9 |
| 2. | Tanaka T. Phase I/II trial for unresectable pancreatic cancer: arterial embolization to achieve a single blood supply for intra-arterial infusion of 5-fluorouracil in combination with full-dose intravenous gemcitabine therapy. Am J Roentgenol 2012;198:1445-1452. |
| 3. | Tanaka T. Intra-arterial chemoinfusion prior to chemoradiotherapy with full-dose systemic gemcitabine for management of locally advanced pancreatic cancer. Anti Cancer Res 2011; 31:3909-3912. |
| 4. | Tanaka T. Pharmacokinetic evaluation of pancreatic arterial infusion chemotherapy after unification of the blood supply in an animal model. J Vasc Interv Radiol 2010; 21:116-21. |
| 5. | Tanaka T. A novel interventional radiology technique for arterial infusion chemotherapy against advanced pancreatic cancer. Am J Roentgenol 2009; 192:w168-187. |
奈良医大での大腸癌に対する研究成果 (一部抜粋)
| 1. | Nishiofuku H, et al. Intraarterial Therapy Using Micellar Nanoparticles Incorporating SN-38 in a Rabbit Liver Tumor Model.J Vasc Interv Radiol 2017;28:457-464 |
| 2. | Tanaka T, et al. Repeated bland-TAE using small microspheres injected via an implantable port-catheter system for liver metastases: an initial experience. Cardiovasc Intervent Radiol. 2014 Apr;37(2):493-7. |
| 3. | Nishiofuku H, et al. Transcatheter arterial chemoembolization using cisplatin powder mixed with degradable starch microspheres for colorectal liver metastases after FOLFOX failure: results of a phase I/II study. J Vasc Interv Radiol. 2013 Jan;24(1):56-65. |
| 4. | Nishiofuku H, et al. Cellular Imaging Using Equivalent Cross-Relaxation Rate Technique in Rabbit VX-2 Tumor Model. Cancer Inform. 2011;10:227-32. |
| 5. | Nishiofuku H, et al. Hepatic arterial infusion of 5-fluorouracil for patients with liver metastases from colorectal cancer refractory to standard systemic chemotherapy: a multicenter, retrospective analysis. Clin Colorectal Cancer. 2010 Dec;9(5):305-10. |
| 6. | Marugami N, et al. Early detection of therapeutic response to hepatic arterial infusion chemotherapy of liver metastases from colorectal cancer using diffusion-weighted MR imaging. Cardiovasc Intervent Radiol. 2009 Jul;32(4):638-46. |
